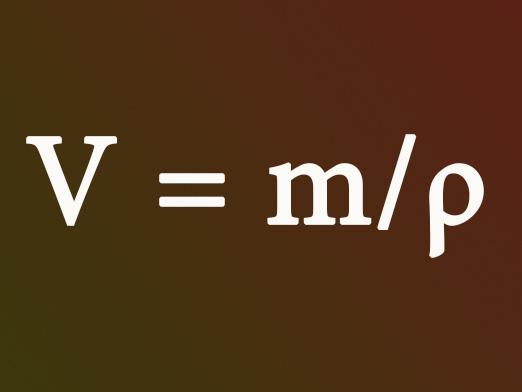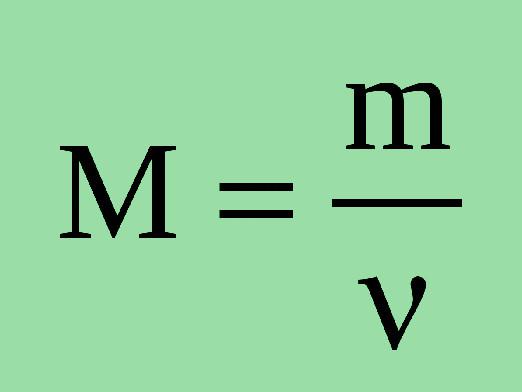Hvordan finder du mængden af et stof?
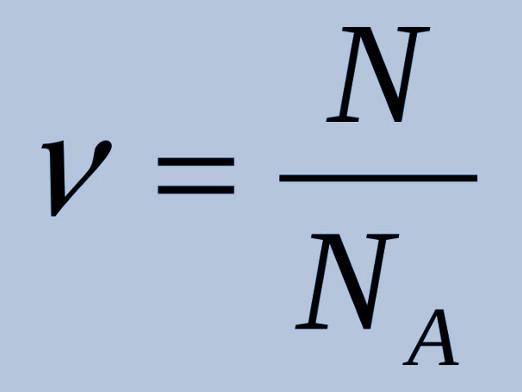
Ved lære af kemi i skolen lærer de at løse forskelligeOpgaver, hvoraf mange er opgaverne til beregning af mængden af materie. Det er imidlertid ikke let at forstå dette materiale, så hvis du har brug for at vide, hvordan man finder mængden af et stof, hjælper vi dig med at forstå dette. Så overvej alt i orden.
Hvad er mængden af materie?
Mængden af et stof er en mængde derkarakteriserer antallet af strukturelle enheder af samme type stof. Strukturelle enheder kan være forskellige partikler: molekyler, atomer, ioner, elektroner. Mængden af materiel i en speciel enhed måles - mol. Beregning i strukturelle enheder er meget ubelejligt, da selv en lille mængde stof indeholder mange sådanne elementer, hvorfor en speciel måleenhed blev opfundet, som vi allerede ved, kaldes en mol. 1 mol indeholder et vist antal enheder af stof, kaldet Avogadro nummeret (konstant Avogadro). Konstant Avogadro: NEn = 6,022 141 79 (30) · 1023 mol-1.
Enheden af mol er meget bekvemt og bredtDet bruges i fysik og kemi, især når det er vigtigt at bestemme detaljeret mængden af et stof op til den mikroskopiske tilstand. Når man for eksempel beskriver kemiske reaktioner, er det mere hensigtsmæssigt og mere præcist at bruge mængden af et stof. Dette er elektrolyse, termodynamik, forskellige kemiske reaktioner, ligninger med en ideel gas mv.
Nøjagtig beregning af mængden af et stof er nødvendigt,for eksempel til kemiske reaktioner, der involverer gasser. Derfor er spørgsmålet om, hvordan man finder mængden af et gasstof, meget vigtigt. Nedenfor betragter vi dette spørgsmål, når vi giver formlen til beregning af gassen.
Kemi: hvordan man finder mængden af materie
For at beregne mængden af et stof, brug følgende formel: n = m / M.
- n er mængden af stof
- m er stoffets masse
- M er stoffets molære masse
Den molære masse er den masse af materie, der tegner sig for en mol af stoffet. Molmassen er lig med produktet af molekylmassen ved hjælp af Avogadro-nummeret.
For gasformige stoffer kan mængden af gas bestemmes efter volumen: n = V / Vm
- n er mængden af stof
- V er volumenet af gas under normale forhold
- Vm - molmængden af gas under normale forhold (lig med 22,4 liter / mol).
Ved at kombinere dataene opnås en formel, der indeholder alle beregninger:
n = m / M = V / Vm = N / NEn
Eksempler på hvordan man finder mængden af et stof, duDu kan se her. Som du kan se, at beregne mængden af stoffet er ikke så svært, det vigtigste - det er rigtigt at bestemme massen af stoffet eller dets volumen (for gasser), og derefter beregnet ved de foreslåede formler, dividere med de konstante data (hver substans har en konstant molær masse eller en permanent molære volumen).